한미약품은 지난 4일(현지시각) 미국 FDA로부터 HM17321(LA-UCN2)의 임상시험계획(IND)을 승인받았다. 이번 임상은 건강한 성인과 비만 환자를 대상으로 안전성, 내약성, 약동학 및 약력학 특성을 평가한다.
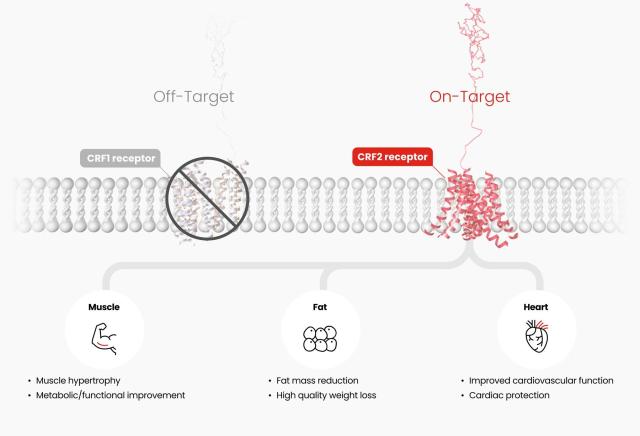
HM17321은 기존 GLP-1 계열 약물과 달리 CRF2 수용체를 선택적으로 타깃하는 UCN2 유사체로, 지방만 선택적으로 줄이면서 근육량과 기능을 증가시키는 새로운 기전의 ‘퍼스트 인 클래스(First-in-Class)’ 신약이다.
펩타이드 기반으로 설계돼 피하 투여가 가능하고 기존 인크레틴 계열 약물과 병용 시 한 번에 투약할 수 있어 환자 편의성이 높다.
한미약품은 이번 신약을 포함한 ‘H.O.P(Hanmi Obesity Pipeline)’을 통해 6개 비만 치료 파이프라인을 구축했으며 2031년 상용화를 목표로 임상개발을 가속화할 계획이다.
최인영 한미약품 R&D센터장은 “HM17321은 단순한 체중 감량이 아니라 지방 감소·근육 증가·대사 개선을 동시에 지향하는 혁신 치료제”라며 “비만을 대사질환 관점에서 접근해 환자 중심의 맞춤형 솔루션을 제시할 것”이라고 말했다.





















댓글 더보기